Menurut sobat apa yang dimaksud dengan reaksi penetralan asam-basa? Apa yang terjadi jika asam direaksikan dengan basa?
Di dalam air, asam kuat terurai membentuk ion H+ dan ion sisa asam. Keberadaan ion H+ dalam larutan asam ditunjukkan oleh nilai pH yang rendah
(pH = –log [H+] < 7).
Dalam larutan basa akan terbentuk ion OH– dan ion sisa basa. Keberadaan ion OH– dalam larutan basa ditunjukkan oleh nilai pH yang tinggi
(pH = 14 – pOH > 7).
Jika larutan asam dan basa dicampurkan akan terjadi reaksi penetralan ion H+ dan OH–. Bukti terjadinya reaksi penetralan ini ditunjukkan oleh nilai pH mendekati 7 (pH ≈ 7).
Nilai pH ≈ 7 menunjukkan tidak ada lagi ion H+ dari asam dan ion OH– dari basa selain ion H+ dan OH– hasil ionisasi air. Dengan demikian, pada dasarnya reaksi asam basa adalah reaksi penetralan ion H+ dan OH–. Persamaan reaksi molekulernya:
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(l)
Persamaan reaksi ionnya: H+(aq)+ Cl–(aq)+ Na+(aq)+OH–(aq) → Na+(aq)+ Cl–(aq)+ H2O(l)
Persamaan ion bersihnya: H+(aq) + OH–(aq) → H2O(l)
Reaksi
asam basa disebut juga reaksi penggaraman sebab dalam reaksi asam basa
selalu dihasilkan garam. Pada reaksi HCl dan NaOH dihasilkan garam dapur
(NaCl). Beberapa contoh reaksi penetralan asam basa atau reaksi
pembentukan garam sebagai berikut:
a. H2SO4(aq) + Mg(OH)2(aq) →MgSO4(aq) + 2H2O(l)
b. HNO3(aq) + Ca(OH)2(aq) →Ca(NO3)2(aq) + H2O(l)
c. HCl(aq) + NH4OH(aq) →NH4Cl(aq) + H2O(l)
Jumat, 20 November 2015
Persamaan Ion dan Molekul
Persamaan reaksi ini disebut persamaan molekuler sebab zat-zat yang bereaksi ditulis dalam bentuk molekul. Persamaan molekul tidak memberikan petunjuk bahwa reaksi itu melibatkan ion-ion dalam larutan, padahal Ca(OH)2 dan Na2CO3 di dalam air berupa ion-ion. Ion-ion yang terlibat dalam reaksi tersebut adalah ion Ca2+ dan ion OH– yang berasal dari Ca(OH)2, serta ion Na+ dan ion CO32– yang berasal dari Na2CO3. Persamaan reaksi dalam bentuk ion ditulis sebagai berikut.
2Na+(aq) + CO32–(aq) + Ca2+(aq) + 2OH–(aq)→ 2Na+(aq ) + 2OH–(aq) + CaCO3(s)
Persamaan ini dinamakan persamaan ion, yaitu suatu persamaan reaksi yang melibatkan ion-ion dalam larutan . Petunjuk pengubahan persamaan molekuler menjadi persamaan ion adalah sebagai berikut:
- Zat-zat ionik, seperti NaCl umumnya ditulis sebagai ion-ion. Ciri zat ionik dalam persamaan reaksi menggunakan fasa (aq) .
- Zat-zat yang tidak larut (endapan) ditulis sebagai rumus senyawa. Ciri dalam persamaan reaksi dinyatakan dengan fasa (s) .
Sehingga persamaan dapat ditulis menjadi:
Ca2+(aq) + CO32–(aq) →CaCO3(s)
Persamaan ini dinamakan persamaan ion bersih. Dalam hal ini, ion OH– dan ion Na+ tergolong ion-ion spektator.
Reaksi Pengendapan
Reaksi dalam larutan tergolong reaksi pengendapan jika salah satu produk reaksi tidak larut di dalam air. Contoh zat yang tidak larut di dalam air, yaitu CaCO3 dan BaCO3. Untuk mengetahui kelarutan suatu zat diperlukan pengetahuan empirik sebagai hasil pengukuran terhadap berbagai zat. Perhatikanlah reaksi antara kalsium klorida dan natrium fosfat berikut.3CaCl2 + 2Na3PO4 → Ca3(PO4)2 + 6NaCl
NaCl akan larut di dalam air, sedangkan Ca3(PO4)2 tidak larut. Senyawa-senyawa fosfat sebagian besar larut dalam air, kecuali senyawa fosfat dari natrium, kalium, dan amonium. Oleh karena itu, persamaan reaksi dapat ditulis sebagai berikut.
3CaCl2(aq) + 2Na3PO4(aq) → Ca3(PO4)2(s) + 6NaCl(aq)
Dengan menghilangkan ion-ion spektator dalam persamaan reaksi itu, perasamaan ion bersih dari reaksi dapat diperoleh.
3Ca2+(aq) + 2PO43–(aq) → Ca3(PO4)2(s)
Reaksi Pembentukan Gas
Reaksi kimia dalam larutan, selain dapat membentuk endapan juga ada yang menghasilkan gas. Misalnya, reaksi antara natrium dan asam klorida membentuk gas hidrogen. Persamaan reaksinya:
Na(s) + 2HCl(aq) → 2NaCl(aq) + H2(g)
Beberapa reaksi yang menghasilkan gas:
- Na2CO3(aq) + 2HCl(aq)→ 2NaCl(aq) + H2O(l) + CO2(g)
- Na2S(aq) + 2HCl(aq)→ 2NaCl(aq) + H2S(g)
- Na2SO3(aq) + 2HCl(aq)→ 2NaCl(aq) + H2O(l) + SO2(g)
teori asam basa
A. MENURUT ARRHENIUS
Asam ialah senyawa yang dalam larutannya dapat menghasilkan ion H+.
Basa ialah senyawa yang dalam larutannya dapat menghasilkan ion OH-.
Contoh:
1) HCl(aq) → H+(aq) + Cl-(aq)
2) NaOH(aq) → Na+(aq) + OH-(aq)
B. MENURUT BRONSTED-LOWRY
Asam ialah proton donor, sedangkan basa adalah proton akseptor.
Contoh:
1) HAc(aq) + H2O(l) ↔ H3O+(aq) + Ac-(aq)
asam-1 basa-2 asam-2 basa-1
HAc dengan Ac- merupakan pasangan asam-basa konjugasi.
H3O+ dengan H2O merupakan pasangan asam-basa konjugasi.
2) H2O(l) + NH3(aq) ↔ NH4+(aq) + OH-(aq)
asam-1 basa-2 asam-2 basa-1
H2O dengan OH- merupakan pasangan asam-basa konjugasi.
NH4+ dengan NH3 merupakan pasangan asam-basa konjugasi.
Eksponen Hidrogen
Besarnya konsentrasi ion H+ dalam larutan disebut derajat keasaman. Untuk menyatakan derajat keasaman suatu larutan dipakai pengertian pH.
pH = – log [H+]
Untuk air murni (25oC): [H+] = [OH-] = 10-7 mol/l
pH = – log 10-7 = 7
Atas dasar pengertian ini, ditentukan:
- Jika nilai pH = pOH = 7, maka larutan bersifat netral
- Jika nilai pH < 7, maka larutan bersifat asam - Jika nilai pH > 7, maka larutan bersifat basa
- Pada suhu kamar: pKw = pH + pOH = 14
Untuk menyatakan nilai pH suatu larutan asam, maka yang paling awal harus ditentukan (dibedakan) antara asam kuat dengan asam lemah.
a. pH Asam Kuat
Bagi asam-asam kuat ( a = 1), maka menyatakan nilai pH larutannya dapat dihitung langsung dari konsentrasi asamnya (dengan melihat valensinya).
Contoh:
1. Hitunglah pH dari 100 ml larutan 0.01 M HCl !
Jawab:
HCl(aq) → H+(aq) + Cl-(aq)
[H+] = [HCl] = 0.01 = 10-2 M
pH = – log 10-2 = 2
2. Hitunglah pH dari 2 liter larutan 0.1 mol asam sulfat !
Jawab:
H2SO4(aq) → 2 H+(aq) + SO42-(aq)
[H+] = 2[H2SO4] = 2 x 0.1 mol/2.0 liter = 2 x 0.05 = 10-1 M
pH = – log 10-1 = 1
b. pH Asam Lemah
Bagi asam-asam lemah, karena harga derajat ionisasinya ¹ 1 (0 < a < 1) maka besarnya konsentrasi ion H+ tidak dapat dinyatakan secara langsung dari konsentrasi asamnya (seperti halnya asam kuat). Langkah awal yang harus ditempuh adalah menghitung besarnya [H+] dengan rumus [H+] = √ ( M . Ka) dimana: M = konsentrasi asam lemah Ka = tetapan ionisasi asam lemah Contoh: Hitunglah pH dari 0.025 mol CH3COOH dalam 250 ml larutannya, jika diketahui Ka = 10-5 Jawab: M = 0.025 mol/0.025 liter = 0.1 M = 10-1 M [H+] = √ (M . Ka) = 10-1 . 10-5 = 10-3 M pH = -log 10-3 = 3 Prinsip penentuan pH suatu larutan basa sama dengan penentuan pH larutam asam, yaitu dibedakan untuk basa kuat dan basa lemah. 1. pH Basa Kuat Untuk menentukan pH basa-basa kuat (a = 1), maka terlebih dahulu dihitung nilai pOH larutan dari konsentrasi basanya. Contoh: a. Tentukan pH dari 100 ml larutan KOH 0.1 M ! b. Hitunglah pH dari 500 ml larutan Ca(OH)2 0.01 M ! Jawab: a. KOH(aq) → K+(aq) + OH-(aq) [OH-] = [KOH] = 0.1 = 10-1 M pOH = – log 10-1 = 1 pH = 14 – pOH = 14 – 1 = 13 b. Ca(OH)2(aq) → Ca2+(aq) + 2 OH-(aq) [OH-1] = 2[Ca(OH)2] = 2 x 0.01 = 2.10-2 M pOH = – log 2.10-2 = 2 – log 2 pH = 14 – pOH = 14 – (2 – log 2) = 12 + log 2 2. pH Basa Lemah Bagi basa-basa lemah, karena harga derajat ionisasinya ¹ 1, maka untuk menyatakan konsentrasi ion OH- digunakan rumus: [OH-] = √ (M . Kb) dimana: M = konsentrasi basa lemah Kb = tetapan ionisasi basa lemah Contoh: Hitunglah pH dari 100 ml 0.001 M larutan NH4OH, jika diketahui tetapan ionisasinya = 10-5 ! Jawab: [OH-] = √ (M . Kb) = 10-3 . 10-5 = 10-4 M pOH = – log 10-4 = 4 pH = 14 – pOH = 14 – 4 = 10 Stoikiometri reaksi dan Titrasi Asam – Basa Persamaan ion Contoh : Reaksi rumus : 2NaOH(aq) + H2SO4(aq) → Na2SO4(aq) + 2H2O(l) Reaksi ion : 2Na+ + 2OH- + 2H+ + SO42- → 2Na+ + SO42- + 2H2O Reaksi bersih : 2H2O(aq) → 2H2O(l) Titrasi Titrasi adalah cara penetapan kadar suatu larutan dengan menggunakan larutan standar yang sudah diketahui konsentrasinya. Motode ini banyak dilakukan di laboratorium. Beberapa jenis titrasi, yaitu: 1. titrasi asam-basa 2. titrasi redoks 3. titrasi pengendapan Contoh: 1. Untuk menetralkan 50 mL larutan NaOH diperlukan 20 mL larutan 0.25 M HCl. Tentukan kemolaran larutan NaOH ! Jawab: NaOH(aq) + HCl(aq) NaCl(aq) + H2O(l) mol HCl = 20 x 0.25 = 5 m mol Berdasarkan koefisien reaksi di atas. mol NaOH = mol HCl = 5 m mol M = n/V = 5 m mol/50mL = 0.1 M 2. Sebanyak 0.56 gram kalsium oksida tak murni dilarutkan ke dalam air. Larutan ini tepat dapat dinetralkan dengan 20 mL larutan 0.30 M HCl.Tentukan kemurnian kalsium oksida (Ar: O=16; Ca=56)! Jawab: CaO(s) + H2O(l) Ca(OH)2(aq) Ca(OH)2(aq) + 2 HCl(aq) CaCl2(aq) + 2 H2O(l) mol HCl = 20 x 0.30 = 6 m mol mol Ca(OH)2 = mol CaO = 1/2 x mol HCl = 1/2 x 6 = 3 m mol massa CaO = 3 x 56 = 168 mg = 0.168 gram Kadar kemurnian CaO = 0.168/0.56 x 100% = 30% Eksponen Hidrogen (pH) A : asam kuat B : basa lemah C : garam D : air (Reaksi Asam – Basa) A + B → C + D m : 1 0,5 - - r : 0,5 0,5 0,5 0,5 s : 0,5 - 0,5 0,5 [H+] = (mol sisa)⁄(volum total) (Reaksi Buffer) A + B → C + D m : 0,5 1 - - r : 0,5 0,5 0,5 0,5 s : - 0,5 0,5 0,5 [H+] = Ka x (mol asam)/(mol garam × valensi ) (Reaksi Hidrolisis) A + B → C + D m : 0,5 0,5 - - r : 0,5 0,5 0,5 0,5 s : - - 0,5 0,5 [H+] = √(Kw/Kb×Garam ×valensi) Jika, A : asam lemah B : basa lemah C : garam D : air Dan jika, Ka > Kb, maka
[H+] = √(Kw/Kb×Ka)
Hasil kali kelarutan
KSP = hasil perkalian [kation] dengan [anion] dari larutan jenuh suatu elektrolit yang sukar larut menurut kesetimbangan heterogen.
Kelarutan suatu elektrolit ialah banyaknya mol elektrolit yang sanggup melarut dalam tiap liter larutannya.
Contoh:
AgCl(s) --> Ag+(aq) + Cl-(aq)
K = [Ag+] [Cl-]/[AgCl]
K . [AgCl] = [Ag+][Cl-]
KspAgCl = [Ag+] [Cl-]
Bila Ksp AgCl = 10-10 , maka berarti larutan jenuh AgCl dalam air pada suhu 25oC, Mempunyai nilai [Ag+] [Cl-] = 10-10
1. Kelarutan zat AB dalam pelarut murni (air).
AnB(s) --> nA+(aq) + Bn-(aq)
s --> n.s s
Ksp AnB = (n.s)n.s = nn.sn+1 s = n+i Ksp AnB/nn
dimana: s = sulobility = kelarutan
Kelarutan tergantung pada:
- suhu
- pH larutan
- ada tidaknya ion sejenis
2. Kelarutan zat AB dalam larutan yang mengandung ion sejenis
AB(s) --> A+ (aq) + B- (aq)
s --> n.s s
Larutan AX :
AX(aq) --> A+(aq) + X-(aq)
b --> b b
maka dari kedua persamaan reaksi di atas:
[A+] = s + b = b, karena nilai s cukup kecil bila dibandingkan terhadap nilai b sehingga dapat diabaikan.
[B-1] = s
Jadi : Ksp AB = b . s
Contoh:
Bila diketahui Ksp AgCl = 10-10 ,berapa mol kelarutan (s) maksimum AgCl dalam 1 liter larutan 0.1 M NaCl ?
Jawab:
AgCl(s) --> Ag+(aq) + Cl-(aq)
s --> s s
NaCl(aq) Na+(aq) + Cl-(aq)
Ksp AgCl = [Ag+] [Cl-] = s . 10-1
Maka s = 10-10/10-1 = 10-9 mol/liter
Dari contoh di atas. kita dapat menarik kesimpulan bahwa makin besar konsentrasi ion sojenis maka makin kecil kelarutan elektrolitnya
Untuk suatu garam AB yang sukar larut berlaku ketentuan, jika:
- [A+] x [B-] < Ksp larutan tak jenuh; tidak terjadi pengendapan - [A+] x [B-] = Ksp larutan tepat jenuh; larutan tepat mengendap - [A+] x [B-] > Ksp larutan kelewat jenuh; di sini terjadi pengendapan zat
Contoh:
Apakah terjadi pengendapan CaCO3. jika ke dalam 1 liter 0.05 M Na2CO3 ditambahkan 1 liter 0.02 M CaCl2, dan diketahui harga Ksp untuk CaCO3 adalah 10-6.
Jawab:
Na2CO3(aq) --> 2 Na+(aq) + CO3- (aq)
[CO32-] = 1 . 0.05 / 1+1 = 0.025 M = 2.5 x 10-2 M
CaCl2(aq) --> Ca2+(aq) + 2Cl-(aq)
[Ca2+] = 1 . 0.02 / 1+1 = 0.01 = 10-2 M
maka : [Ca2+] x [CO32-] = 2.5 x 10-2 x 10-2 = 2.5 x 10-4
karena : [Ca2+] x [CO32-] > Ksp CaCO3, maka akan terjadi endapan CaCO3
Sistem Koloid
Sistem koloid (selanjutnya disingkat "koloid" saja) merupakan suatu bentuk campuran (sistem dispersi) dua atau lebih zat yang bersifat homogen namun memiliki ukuran partikel terdispersi yang cukup besar (1 - 100 nm), sehingga terkena efek Tyndall. Bersifat homogen berarti partikel terdispersi tidak terpengaruh oleh gaya gravitasi atau gaya lain yang dikenakan kepadanya; sehingga tidak terjadi pengendapan, misalnya. Sifat homogen ini juga dimiliki oleh larutan, namun tidak dimiliki oleh campuran biasa (suspensi).
Koloid mudah dijumpai di mana-mana: susu, agar-agar, tinta, sampo, serta awan merupakan contoh-contoh koloid yang dapat dijumpai sehari-hari. Sitoplasma dalam sel juga merupakan sistem koloid. Kimia koloid menjadi kajian tersendiri dalam kimia industri karena kepentingannya.
JENIS KOLOID
Sistem koloid digolongkan berdasarkan pada jenis fase terdispersi dan medium pendispersinya.
- koloid yang mengandung fase terdispersi padat disebut sol.
- koloid yang mengandung fase terdispersi cair disebut emulsi.
- koloid yang mengandung fase terdispersi gas disebut buih.
Sifat-sifat Koloid
Efek Tyndall
Efek Tyndall ialah gejala penghamburan berkas sinar (cahaya) oleh partikel-partikel koloid. Hal ini disebabkan karena ukuran molekul koloid yang cukup besar. Efek tyndall ini ditemukan oleh John Tyndall (1820-1893), seorang ahli fisika Inggris. Oleh karena itu sifat itu disebut efek tyndall.
Efek tyndall adalah efek yang terjadi jika suatu larutan terkena sinar. Pada saat larutan sejati disinari dengan cahaya, maka larutan tersebut tidak akan menghamburkan cahaya, sedangkan pada sistem koloid, cahaya akan dihamburkan. hal itu terjadi karena partikel-partikel koloid mempunyai partikel-partikel yang relatif besar untuk dapat menghamburkan sinar tersebut. Sebaliknya, pada larutan sejati, partikel-partikelnya relatif kecil sehingga hamburan yang terjadi hanya sedikit dan sangat sulit diamati.
Gerak Brown
Gerak Brown ialah gerakan partikel-partikel koloid yang senantiasa bergerak lurus tapi tidak menentu (gerak acak/tidak beraturan). Jika kita amati koloid dibawah mikroskop ultra, maka kita akan melihat bahwa partikel-partikel tersebut akan bergerak membentuk zigzag. Pergerakan zigzag ini dinamakan gerak Brown. Partikel-partikel suatu zat senantiasa bergerak. Gerakan tersebut dapat bersifat acak seperti pada zat cair dan gas( dinamakan gerak brown), sedangkan pada zat padat hanya beroszillasi di tempat ( tidak termasuk gerak brown ). Untuk koloid dengan medium pendispersi zat cair atau gas, pergerakan partikel-partikel akan menghasilkan tumbukan dengan partikel-partikel koloid itu sendiri. Tumbukan tersebut berlangsung dari segala arah. Oleh karena ukuran partikel cukup kecil, maka tumbukan yang terjadi cenderung tidak seimbang. Sehingga terdapat suatu resultan tumbukan yang menyebabkan perubahan arah gerak partikel sehingga terjadi gerak zigzag atau gerak Brown.
Semakin kecil ukuran partikel koloid, semakin cepat gerak Brown yang terjadi. Demikian pula, semakin besar ukuran partikel koloid, semakin lambat gerak Brown yang terjadi. Hal ini menjelaskan mengapa gerak Brown sulit diamati dalam larutan dan tidak ditemukan dalam campuran heterogen zat cair dengan zat padat (suspensi). Gerak Brown juga dipengaruhi oleh suhu. Semakin tinggi suhu sistem koloid, maka semakin besar energi kinetik yang dimiliki partikel-partikel medium pendispersinya. Akibatnya, gerak Brown dari partikel-partikel fase terdispersinya semakin cepat. Demikian pula sebaliknya, semakin rendah suhu sistem koloid, maka gerak Brown semakin lambat.
Adsorpsi
Adsorpsi ialah peristiwa penyerapan partikel atau ion atau senyawa lain pada permukaan partikel koloid yang disebabkan oleh luasnya permukaan partikel. (Catatan : Adsorpsi harus dibedakan dengan absorpsi yang artinya penyerapan yang terjadi di dalam suatu partikel). Contoh : (i) Koloid Fe(OH)3 bermuatan positif karena permukaannya menyerap ion H+. (ii) Koloid As2S3 bermuatan negatif karena permukaannya menyerap ion S2.
Muatan koloid
Dikenal dua macam koloid, yaitu koloid bermuatan positif dan koloid bermuatan negatif.
Koagulasi koloid
Koagulasi adalah penggumpalan partikel koloid dan membentuk endapan. Dengan terjadinya koagulasi, berarti zat terdispersi tidak lagi membentuk koloid. Koagulasi dapat terjadi secara fisik seperti pemanasan, pendinginan dan pengadukan atau secara kimia seperti penambahan elektrolit, pencampuran koloid yang berbeda muatan.
Koloid pelindung
Koloid pelindung ialah koloid yang mempunyai sifat dapat melindungi koloid lain dari proses koagulasi.
Dialisis
Dialisis ialah pemisahan koloid dari ion-ion pengganggu dengan cara ini disebut proses dialisis. Yaitu dengan mengalirkan cairan yang tercampur dengan koloid melalui membran semi permeable yang berfungsi sebagai penyaring. Membran semi permeable ini dapat dilewati cairan tetapi tidak dapat dilewati koloid, sehingga koloid dan cairan akan berpisah.
Elektroforesis
Elektroferesis ialah peristiwa pemisahan partikel koloid yang bermuatan dengan menggunakan arus listrik.
link : http://al-kahi.blogspot.co.id/2012/09/materi-kimia-kelas-xi-semester-1.html
Pembuatan dan Kegunaan Unsur Halogen
Apakah sobat sudah mengetahui bagaimana kegunaan dan pembuatan unsur halogen?
Gas F2 merupakan oksidator kuat sehingga hanya dapat dibuat melalui elektrolisis garamnya, yaitu larutan KF dalam HF cair. Dalam elektrolisis dihasilkan gas H2 di katode dan gas F2 di anode. Perhatikan gambar disamping.
Gas F2 diproduksi secara komersial untuk bahan bakar nuklir uranium. Logam uranium direaksikan dengan gas fluorin berlebih menghasilkan uranium heksafluorida, UF6 (padatan berwarna putih dan mudah menguap).
Gas Cl2 dibuat melalui elektrolisis lelehan NaCl, reaksinya:
Anode: Cl–(l) → Cl2(g)
Katode: Na+(l) →Na(s)
Gas Cl2 digunakan sebagai bahan dasar industri plastik, seperti vinil klorida, CH2=CHCl (untuk PVC), CCl4 (untuk fluorokarbon), dan CH3Cl (untuk silikon dan TEL). Dalam jumlah besar, klorin digunakan untuk desinfektan, pemutih, pulp kertas, dan tekstil.
Gas Br2 dibuat dari air laut melalui oksidasi dengan gas Cl2. Secara komersial, pembuatan gas Br2 sebagai berikut.
- Air laut dipanaskan kemudian dialirkan ke tanki yang berada di puncak menara.
- Uap air panas dan gas Cl2 dialirkan dari bawah menuju tanki. Setelah terjadi reaksi redoks, gas Br2 yang dihasilkan diembunkan hingga terbentuk lapisan yang terpisah. Bromin cair berada di dasar tangki, sedangkan air di atasnya.
- Selanjutnya bromin dimurnikan melalui distilasi. Bromin digunakan dalam industri untuk membuat senyawa metil bromida, CH3Br (sebagai pestisida), perak bromida (untuk film fotografi), dan alkali bromida (untuk sedatif).
Sifat dan Pembuatan Senyawa Halogen
Senyawa halogen yang penting adalah asam hidrogen halida (HX), asam okso-halida (HXOn), dan garamnya (MX). Setiap unsur halogen dapat membentuk senyawa biner dengan hidrogen: HF, HCl, HBr, dan HI. Semuanya merupakan gas tak berwarna dengan bau sangat tajam.Titik didih asam halida meningkat dari atas ke bawah dalam sistem periodik (HCl = –85°C; HBr = –67°C; HI = –35°C), kecuali HF memiliki titik didih paling tinggi, yaitu 20°C. Penyimpangan ini sebagai akibat adanya ikatan hidrogen antarmolekul HF yang sangat kuat dibandingkan asam-asam halida yang lain.
Kekuatan asam halida di dalam pelarut air meningkat dari atas ke bawah dalam tabel periodik. Hal ini disebabkan oleh jari-jari atom halogen yang makin besar sehingga kemampuan menarik atom H makin lemah, akibatnya atom H mudah lepas.
Asam-asam halida di dalam air terionisasi sempurna, kecuali asam fluorida tergolong asam lemah dengan derajat ionisasi 2,9%. Persamaan ionisasinya:
Asam-asam halida dapat disintesis langsung dari unsur-unsurnya, seperti berikut ini.
Gas F2 dan H2 bereaksi sangat dahsyat membentuk senyawa HF, tetapi reaksinya tidak memiliki nilai komersial, sebab gas F2 sendiri dibuat dari penguraian HF. H2(g) + F2(g) →2HF(g)
Senyawa HCl dibuat melalui reaksi gas Cl2 dan H2 berlebih. H2(g) + Cl2(g) →2HCl(g)
HBr dan HI dibuat dengan cara serupa, tetapi menggunakan katalis platina sebab reaksi tanpa katalis sangat lambat.
Umumnya, asam-asam halida disintesis melalui pemanasan garam halida dengan asam yang tidak mudah menguap, seperti berikut ini.
HF, dibuat dari garam CaF2 dan asam sulfat pekat. Reaksinya: CaF2(s) + H2SO4(l) →CaSO4(s) + 2HF(g)
HCl, dibuat dari natrium klorida dan asam sulfat pekat. Reaksinya: NaCl(s) + H2SO4(l) →NaHSO4(s) + HCl(g) . Pada suhu tinggi, hasil yang terbentuk adalah natrium sulfat: NaCl(s) + NaHSO4(l) →Na2SO4(s) + HCl(g)
HBr dan HI, tidak dapat dibuat dengan H2SO4, sebab dapat mengoksidasi Br– dan I– menjadi unsur-unsurnya. Dalam hal ini digunakan asam fosfat. Reaksinya: NaBr(s) + H3PO4(l) →HBr(g) + NaH2PO4(s)
Kegunaan utama HF adalah sebagai bahan baku pembuatan CCl3F, freon, dan teflon. Senyawa CCl3F digunakan sebagai pendingin dan bahan bakar aerosol, yang disintesis dari CCl4 dan HF dengan antimon pentafluorida sebagai katalis. Reaksinya: CCl4(l) + HF(g) →CCl3F(aq) + HCl(g)
Kegunaan utama HF yang lain adalah sebagai cairan elektrolit dalam pengolahan mineral aluminium dan untuk melukis/mengetsa gelas. Dalam mengeetsa gelas, HF bereaksi dengan silika (SiO2), kemudian bereaksi dengan gelas. Reaksinya:
Senyawa HCl adalah asam keempat yang penting bagi industri asam setelah asam sulfat, fosfat, dan nitrat. Asam ini digunakan untuk membersihkan permukaan logam dari oksida (disebut pickling) dan untuk mengekstrak bijih logam tertentu, seperti tungsten.
Dalam elektrolisis larutan NaCl, gas Cl2 yang dihasilkan pada anode dapat bereaksi dengan larutan NaOH yang dihasilkan di katode membentuk natrium hipoklorit. Reaksinya:
Cl2(g) + 2NaOH(aq) → NaClO(aq) + NaCl(aq) + H2O(l)
Larutan NaClO digunakan sebagai pemutih pada industri tekstil. Ion hipoklorit tidak stabil, dan terdisproporsionasi membentuk ion klorat, ClO3– dan ion klorida, Cl–. Reaksinya: 3ClO–(aq) → ClO3–(aq) + 2Cl–(aq)
link : http://materi-kimia-sma.blogspot.co.id/2013/12/pembuatan-dan-kegunaan-unsur-halogen.html
Unsur Golongan Alkali
Unsur-unsur golongan IA disebut juga logam alkali. Unsur-unsur alkali merupakan logam yang sangat reaktif. Menurut sobat kenapa unsur golongan alkali sangat reaktif? Kereaktifan unsur alkali disebabkan kemudahan melepaskan elektron valensi pada kulit ns1 membentuk senyawa dengan bilangan oksidasi +1. Oleh sebab itu, unsur-unsur logam alkali tidak ditemukan sebagai logam bebas di alam, melainkan berada dalam bentuk senyawa.
Kelimpahan Unsur Logam Alkali di Alam
Sumber utama logam alkali adalah air laut. Air laut merupakan larutan garam-garam alkali dan alkali tanah dengan NaCl sebagai zat terlarut utamanya. Jika air laut diuapkan, garam-garam yang terlarut akan membentuk kristal.
Selain air laut, sumber utama logam natrium dan kalium adalah deposit mineral yang ditambang dari dalam tanah, seperti halit (NaCl), silvit (KCl), dan karnalit (KCl.MgCl.H2O). Mineral-mineral ini banyak ditemukan di berbagai belahan bumi.
Pembentukan mineral tersebut melalui proses yang lama. Mineral berasal dari air laut yang menguap dan garam-garam terlarut mengendap sebagai mineral. Kemudian, secara perlahan mineral tersebut tertimbun oleh debu dan tanah sehingga banyak ditemukan tidak jauh dari pantai.
Logam alkali lain diperoleh dari mineral aluminosilikat. Litium terdapat dalam bentuk spodumen, LiAl(SiO3)2. Rubidium terdapat dalam mineral lepidolit. Cesium diperoleh dari pollusit yang sangat jarang, CsAl(SiO3)2.H2O. Fransium bersifat radioaktif.
Sifat-Sifat Unsur Logam Alkali
Unsur-unsur alkali semuanya logam yang sangat reaktif dengan sifat-sifat fisika ditunjukkan pada Tabel berikut.Logam alkali sangat reaktif dalam air. Oleh karena tangan kita mengandung air, logam alkali tidak boleh disentuh langsung oleh tangan.
Semua unsur golongan IA berwarna putih keperakan berupa logam padat, kecuali cesium berwujud cair pada suhu kamar. Natrium merupakan logam lunak dan dapat dipotong dengan pisau. Kalium lebih lunak dari natrium.
Pada tabel disamping tampak bahwa logam litium, natrium, dan kalium mempunyai massa jenis kurang dari 1,0 g cm–3. Akibatnya, logam tersebut terapung dalam air. Akan tetapi, ketiga logam ini sangat reaktif terhadap air dan reaksinya bersifat eksplosif disertai nyala.
Sifat-sifat fisika logam seperti lunak dengan titik leleh rendah menjadi petunjuk bahwa ikatan logam antaratom dalam alkali sangat lemah. Ini akibat jari-jari atom logam alkali relatif besar dibandingkan unsur-unsur lain dalam satu periode. Penurunan titik leleh dari litium ke cesium disebabkan oleh jari-jari atom yang makin besar sehingga mengurangi kekuatan ikatan antaratom logam.
Logam-logam alkali merupakan reduktor paling kuat, seperti ditunjukkan oleh potensial reduksi standar yang negatif pada tabel disamping.
Keelektronegatifan logam alkali pada umumnya rendah (cesium
paling rendah), yang berarti logam tersebut cenderung membentuk kation. Sifat ini juga didukung oleh energi ionisasi pertama yang rendah, sedangkan energi ionisasi kedua sangat tinggi sehingga hanya ion dengan biloks +1 yang dapat dibentuk oleh logam alkali.
Semua logam alkali dapat bereaksi dengan air. Reaksinya melibatkan pergantian hidrogen dari air oleh logam membentuk suatu basa kuat disertai pelepasan gas hidrogen. 2Na(s) + 2H2O(l) → 2NaOH(aq) + H2(g)
Kereaktifan logam alkali terhadap air menjadi sangat kuat dari atas ke bawah dalam tabel periodik. Sepotong logam litium jika dimasukkan ke dalam air akan bergerak di sekitar permukaan air disertai pelepasan gas H2. Kalium bereaksi sangat dahsyat disertai ledakan dan nyala api berwarna ungu.
Dalam udara terbuka, logam alkali bereaksi dengan oksigen membentuk oksida. Litium membentuk Li2O, natrium membentuk Na2O, tetapi produk yang dominan adalah natrium peroksida (Na2O2).
Jika kalium dibakar dengan oksigen, produk dominan adalah kalium superoksida (KO2), suatu senyawa berwarna kuning-jingga. Oksida ini merupakan senyawa ion dari ion K+ dan ion O2–.
Logam alkali bereaksi dengan halogen membentuk garam halida. Pada suhu tinggi, logam alkali bereaksi dengan hidrogen membentuk senyawa hidrida, seperti LiH dan NaH. Di udara terbuka, litium dapat bereaksi dengan gas nitrogen, sedangkan logam lainnya tidak dapat bereaksi.
Jika logam alkali atau senyawanya dibakar dalam nyala bunsen, akan tampak warna yang khas untuk setiap logam alkali. Warna-warna tersebut menjadi petunjuk adanya logam alkali di dalam suatu sampel.
link : http://materi-kimia-sma.blogspot.co.id/2013/12/unsur-golongan-alkali.html
Kimia Dasar: Jenis-Jenis Materi
Seperti yang tertulis pada artikel “Apa Sih Ilmu Kimia Itu?”, materi termasuk dalam salah satu hal yang dipelajari dalam ilmu kimia. Meteri sendiri dapat diklasifikasikan dalam 2 kelompok besar, yaitu zat tunggal dan campuran. Kita lihat perbedaannya satu persatu, yuk!
Zat tunggal adalah materi yang mempunya susunan dan sifat yang sama atau homogen. Unsur dan senyawa termasuk dalam kategori zat tunggal ini. Contoh umum zat tunggal yang sering ditemui adalah karbon (C) di pensil kita, logam emas (Au), dan air (H2O). Nah, kalau si karbon C dan si emas Au mudah dikenali sebagai materi dengan susunan yang sama karena hanya terdiri dari karbon C dan Au, namun mengapa air yang rumusnya H2O dimasukkan dalam kategori zat tunggal juga? Mari kita lihat lebih dalam lagi.
Pensil
Unsur didefinisikan sebagai zat yang tidak dapat diuraikan lagi menjadi zat-zat yang lebih sederhana dengan reaksi kimia biasa. Unsur dibagi menjadi 3 sifat, yaitu unsur logam, unsur non-logam, dan unsur metaloid. Unsur logam berbentuk padat, kecuali raksa ya, karena raksa berbentuk cair. Contoh raksa ada di termometer yang sering digunakan untuk mengukur suhu. Unsur logam juga dapat menghantarkan listrik dan memiliki kilap. Contoh unsur logam adalah emas (Au), perak (Ag), dan tembaga (Cu).
Emas
Sumber: radioinformasi.com
Unsur non-logam dapat berbentuk padat seperti belerang (S), cairan seperti bromida (Br), atau gas seperti hidrogen (H). Unsur non-logam tidak dapat menghantar listrik, kecuali karbon (C), dan tidak memiliki kilap logam, kecuali karbon (C).
Unsur metaloid adalah unsur yang memiliki sifat logam dan non-logam. Unsur ini sifatnya semikonduktor, tidak seperti 2 unsur lain yang secara pasti merupakan konduktor dan bukan konduktor. Contoh unsur metaloid adalah boron (B), silikon (Si), germanium (Ge), arsen (As), antimon (Sb), telurium (Te), dan polonium (Po). Sifat unsur ini lebih rapuh dari unsur logam namun lebih kuat daripada unsur non-logam dan beberapa metaloid memiliki sifat kilap seperti logam.
Nah, selain unsur, masih ada senyawa. Apa itu senyawa? Senyawa adalah suatu zat yang dihasilkan dari gabungan secara kimia dua atau lebih unsur sehingga senyawa dapat diuraikan menjadi zat yang lebih sederhana. Dalam senyawa, ada yang disebut sebagai Hukum Perbandingan Tetap, yaitu perbandingan massa masing-masing unsur dalam senyawa adalah tetap. Contoh senyawa adalah air dan gula-gula sederhana. Air tersusun dari unsur hidrogen dan unsur oksigen sehingga dimasukkan dalam kategori senyawa. Gula tersusun atas unsur karbon, hidrogen, dan oksigen, juga termasuk dalam kategori senyawa.
Sekarang kita bahas kelompok materi berikutnya, yaitu campuran. Campuran merupakan materi homogen atau heterogen yang terbentuk dari dua atau lebih zat tunggal yang berbeda. Kalian pasti suka minum es teh manis? Atau kopi manis? Dua minuman tersebut termasuk dalam campuran, karena merupakan campuran air dengan gula maupu kopi dengan gula. Campuran sendiri dibedakan lagi menjadi beberapa jenis, yaitu larutan, suspensi, emulsi, dan koloid.
Apa itu larutan? Larutan merupakan campuran yang membentuk 1 keadaan atau fase, baik fase cair, padat, maupun gas, dan sifatnya homogen. Contohnya adalah air dengan gula dan gas nitrogen dalam gas hidrogen.
Suspensi berbeda dengan larutan dalam hal fase yang dibentuk, karena suspensi dapat membentuk 2 atau lebih fase, sedangkan larutan hanya 1 fase. Contohnya adalah air dengan tepung dan bensin dengan garam. Contoh yang sering kita temui adalah darah. Darah terdiri dari campuran sel darah dan platelet, dan dapat dipisah melalui suatu teknik sentrifugasi.
Suspensi darah
Sumber: beltina.org
Ada lagi emulsi, yaitu campuran yang dalam bentuk suspensi cair dikocok. Butiran zat cair dalam emulsi akan berada di antara zat cair lainnya. Contohnya adalah minyak dengan air. Jika kita mengocok campuran minyak dan air, akan terlihat butiran-butiran yang terpisah, bukan? Nah, itulah emulsi.
Yang terakhir adalah koloid. Bila ada campuran yang terlihat homogen namun sebenarnya ada satu fase dalam fase lain, itu disebut koloid. Contoh koloid adalah kabut, dimana kabut sebenarnya adalah uap air yang terdapat dalam udara. Contoh lain adalah busa sabun, yaitu gas dalam air.
SOTO SEGER MBOK GIYEM BOYOLALI
Soto Seger Mbok Giyem mempunyai kedudukan penting dalam peta kuliner Boyolali. Boleh dibilang ia adalah penanda kebangkitan usaha kuliner di Boyolali. Kemunculannya seolah menggairahkan kembali dan makin menyemarakkan dunia kuliner di kota kecil ini.
Soto Seger Mbok Giyem mampu menarik banyak pelanggan baik dari dalam maupun luar kota. Alhasil di dekat warungnya pun mulai banyak bermunculan penjual makanan seperti bubur sambal lethok (sambal tumpang khas Boyolali), bakso, susu segar, bothok, steak, dsb. Warung-warung makan yang sudah lama berdiri pun turut bergairah kembali.
Sebelum kemunculan Soto Seger Mbok Giyem, sangat sulit untuk menemukan tempat jajan yang enak di Boyolali. Dulu yang terkenal barangkali hanya Soto Rumput dan bubur tumpang Mbah Merto di dekat terminal. Tapi sekarang pilihannya sudah semakin banyak, bahkan kalau malam ada banyak warung tenda yg menjajakan bubur tumpang, opor, kare ayam, susu segar, dsb.
Lantas apa yang istimewa dari soto ini? Soto Seger memiliki kuah bening yang rasanya gurih dan menyegarkan, sesuai dengan namanya. Disini tersedia soto ayam dan soto daging sapi, tapi yang paling populer adalah soto sapinya. Soto disajikan dalam mangkuk kecil dengan isian daging sapi/suwiran ayam, kecambah, ditambah taburan daun seledri dan bawang merah goreng. Untuk soto ayam biasanya ada tambahan keripik kentang di dalamnya.
Makan soto di warung ini makin istimewa karena di meja anda akan menemukan deretan panjang makanan kecil / lauk pendamping untuk soto. Ada sate ayam, sate kikil, sate babat, Sate paru, sate udang tepung, sate cingur, sate telur puyuh, sate uritan, sate hati-ampela ayam, dan berbagai macam gorengan seperti tempe goreng, mendoan, tahu bakso, bakwan sayur, sosis Solo, mentho (makanan kecil khas boyolali yang terbuat dari kacang, singkong, dan kelapa), dll. Tempe gorengnya enak, sangat renyah sampai ke dalam.
Sate uritan di Soto Seger Mbok Giyem
Di Boyolali, Soto Seger Mbok Giyem memiliki kurang lebih empat cabang. Warung yang pertama kali berdiri ada di Jalan Garuda, sebelah Selatan Pasar Sunggingan. Lokasinya agak masuk ke dalam, kurang lebih 20 m dari jalan raya. Dua cabang lainnya ada di Jalan Pandanaran, jalan utama di Boyolali, sehingga mudah ditemukan. Cabang yang satunya lagi ada di seberang RSU Pandan Arang. Soto Seger Mbok Giyem juga sudah membuka cabang di Solo, lokasinya dekat Lottemart.
Jam buka: 06.00 – 18.00 (jam buka bervariasi tergantung cabangnya). Kalau yang di Jl. Pandanaran siang hari biasanya sudah habis.
Lokasi:
- Warung Soto Seger Mbok Giyem Boyolali 1: Jalan Garuda, selatan Pasar Sunggingan (yang ada patung sapinya). Warungnya berhadapan dengan SDN 5 Boyolali
- Warung Soto Seger Mbok Giyem Boyolali 2 & 4: Jalan Pandanaran. Warungnya cukup besar dan tepat berada di pinggir jalan.
- Warung Soto Seger Mbok Giyem Boyolali 3: Seberang RSU Pandan Arang Boyolali.
TEMPAT MENARIK di BOYOLALI
Tempat Wisata Menarik di Boyolali
Tidak salah. Boyolali memang sangat terkenal sebagai kota susu. Kafe-kafe serta warung tenda di Solo dan Jogja yang menjadikan susu sebagai menu unggulan sangat mengandalkan produksi susu dari Boyolali
Hal lain yang langsung terlintas di pikiran ketika membicarakan kabupaten Boyolali adalah hawanya yang sejuk bahkan cenderung dingin di beberapa wilayah. Hal ini dikarenakan kabupaten ini terletak di kaki dua gunung yang saling bertetangga: Merapi dan Merbabu
Lokasi Kabupaten Boyolali sangat strategis karna berada di tengah-tengah antara kota Semarang, Solo, Jogja serta Magelang. Sebagaimana sebuah daerah yang terletak di kaki gunung, Boyolali punya banyak sekali tempat wisata berhawa sejuk yang sangat pantas untuk dikunjungi. Berikut ini adalah 9 tempat paling menarik yang bisa dikunjungi di Boyolali
1. New Selo dan Trekking Gunung Merapi
Foto: https://journeysoflenongers.wordpress.com
New Selo adalah salah satu tempat terbaik untuk menikmati kemegahan Gunung Merbabu. Dari tempat ini kita bisa menyaksikan pemandangan gunung Merbabu yang berdiri begitu gagah di depan mata. Lokasi New Selo yang berada di ketinggian memungkinkan kita untuk menyaksikan pemandangan hijau dari atas sana
New Selo merupakan jalur yang dilewati saat melakukan pendakian Gunung Merapi. Di tempat ini terdapat warung-warung yang menyediakan berbagai minuman serta makanan. Para pendaki yang baru saja melakukan pendakian biasanya akan mampir kesini untuk memesan minuman hangat sambil meluruskan kaki
2. Trekking Gunung Merbabu
Gunung Merbabu merupakan sebuah gunung yang menjadi salah satu tujuan favorite para pecinta alam untuk melakukan pendakian. Lokasi gunung ini berada di antara kabupaten Boyolali, Magelang, serta Kota Salatiga. Salah satu jalur pendakian ke gunung ini adalah melalui jalur Selo di Boyolali
Menurut beberapa pendaki, pendakian Gunung Merbabu melalui jalur Selo adalah yang paling mengesankan karna memiliki pemandangan paling indah. Jika melakukan pendakian dari jalur Selo kita akan melewati beberapa padang sabana luas yang dipenuhi oleh bunga edelweis.
3. Candi Lawang
Foto: https://kartuwayang.wordpress.com/
Dalam Bahasa Jawa lawang artinya pintu. Nama ini diambil karna candi ini memiliki bentuk pintu yang sangat mencolok.
Candi Lawang merupakan sebuah candi bercorak Hindu yang diperkirakan dibangun pada abad ke-9. Candi ini sangat berbeda dengan candi-candi pada umumnya karna disana tidak ditemui arca maupun relief. Yang ada di candi ini hanyalah tumpukan batu-batu berornamen. Beberapa masih berserakan dan belum tertata. Lokasi Candi Lawang berada di belakang sebuah rumah. Candi ini berada di Dusun Gedangan, Kecamatan Cepogo
4. Candi Sari
Foto: kaskus
Lokasi candi ini juga berada di Desa Gedangan, Kecamatan Cepogo. Candi Sari merupakan sebuah candi Hindu yang lokasinya berada di atas bukit. Oleh masyarakat setempat, bukit dimana candi ini berada dipercaya sebagai sumber mata air yang digunakan untuk kebutuhan sehari-hari masyarakat setempat. Oleh karenanya, situs sejarah ini dikeramatkan oleh warga
Lokasi bukit sendiri dikelilingi oleh beberapa desa antara lain Candirejo, Candisari dan Josari. Beberapa warga disana memegang sebuah kepercayaan tertentu untuk menjaga kelestarian situs bersejarah tersebut. Candi Sari sendiri pertama kali ditemukan pada tahun 1967
5. Waduk Bade
Foto: https://aryoblackstar.wordpress.com/
Waduk Bade merupakan sebuah tempat wisata lokal yang cukup menarik di Boyolali. Berkunjung ke tempat ini saat hari beranjak senja merupakan sebuah pilihan yang sangat pas karna pemandangan sunset yang disajikan waduk ini sangat keren. Gunung Merbabu dan Gunung Merapi akan terlihat begitu mungil dari tempat ini
Waduk Bade berada di desa Bade, kecamatan Klego. Konon, lokasi waduk ini berada di tengah-tengah kecamatan Klego yang sebagian wilayahnya merupakan area pertanian. Sehingga keberadaan waduk ini bisa mengairi sawah-sawah tersebut. Waduk Klego merupakan salah satu lokasi favorite warga sekitar yang memiliki hobby memancing
6. Waduk Kedung Ombo
Kedung Ombo adalah sebuah waduk besar yang lokasinya masuk dalam dalam wilayah tiga kabupaten yakni Boyolali, Sragen serta Grobogan. Di bagian Boyolali, waduk berada di Desa Wonoharjo, Kecamatan Kemusu. Jaraknya kira-kira 50 km dari kota Boyolali ke arah utara. Selain berfungsi untuk mengairi persawahan, waduk ini juga punya objek wisata yang sangat menarik
Di area wisata Gedung Ombo kita akan melihat pemandangan rumput hijau yang sangat luas dan begitu mengesankan. Selain itu, di sekitar area wisata juga terdapat pasar ikan tradisional. Disana kita bisa memesan ikan bakar yang ikannya diambil langsung dari waduk sehingga masih segar. Ada juga beberapa fasilitas penunjang lain seperti camping ground, tempat pemancingan serta hutan wisata
7. Waduk Cengklik
Foto: http://mblusuk.com/
Meski masuk wilayah kabupaten Boyolali, Namun lokasi waduk ini lebih dekat dengan kota Solo. Dari kota Solo lokasi waduk ini bisa ditempuh sekitar 20 menit naik kendaraan bermotor. Melewati bandara Adi Sumarmo
Waduk Bade menjadi salah satu tempat nongkrong favorite anak-anak muda saat sore hari. Terutama penggemar fotografi karna pemandangan sunset di waduk ini sangat bagus. Gunung Merbabu dan Gunung Merapi juga akan tampak begitu mungil dari waduk ini. Di Waduk Cengklik kita akan bisa menyaksikan beberapa orang yang sedang memancing. Sembari menikmati suasana sore, kita bisa membeli makanan murah meriah seperti cilok yang biasanya banyak dijajakan di sekitar waduk
8. Pemandian Umbul Pengging
Foto: http://malikfa.blogspot.com/
Melihat kondisi air yang sangat jerih di pemandian ini niscaya akan membuat siapapun tak tahan untuk segera menceburkan diri ke dalamnya. Dasaran kolam yang berupa batu-batu halus terlihat begitu jelas
Pemandian Pengging ini berada di kecamatan Banyudono. Sekitar 20 menit jika ditempuh dari Kota Solo. Tempat ini cukup spesial karna dulunya merupakan tempat pemandian keluarga Kraton Kasunanan Solo. Sehingga jangan heran kalau di sekitar sana masih terdapat bangunan-bangunan yang bernuansa kraton. Di sekitar pemandian juga terdapat makam seorang pujangga kraton bernama Raden Ngabehi Yosodipuro
9. Taman Air Tlatar
Tlatar merupakan tempat rekreasi keluarga yang cukup terkenal di Boyolali. Setiap akhir pekan tempat ini selalu ramai. Pengunjungnya tidak hanya warga Boyolali namun juga dari beberapa kota di sekitarnya seperti Klaten serta Solo. Di Tlatar ini kita bisa menikmati sajian kuliner sambil bermain air
Sebagai sebuah ekowisata, Tlatar memiliki nuansa alam yang begitu terasa. Fasilitas dan wahana yang dimiliki pun cukup lengkap. Selain tempat bermain yang diberi nama “Kolam Keceh”, ada juga wahana berupa kolam renang untuk anak-anak, becak air serta terapi ikan
link : http://www.yukpiknik.com/destinasi/tempat-wisata-boyolali/
KULINER KHAS BOYOLALI
Nasi Urap Sambal Tumpang di Warung Soto Nggoper Boyolali
Jika membaca judul di atas anda pasti menangkap hal yang aneh, di warung soto kok makannya sambal tumpang? Tapi memang begitulah adanya. Meski menggunakan nama warung soto, tempat ini juga menyediakan menu nasi urap (sega gudhang) dan sambal tumpang (orang Boyolali menyebutnya sambal lethok) yang popularitasnya bahkan mengalahkan menu sotonya.
Urap khas Boyolali (orang Jawa menyebutnya gudhangan) terasa istimewa karena di atasnya ditambahkan taburan bubuk kacang yang memunculkan citarasa khas nan sedap. Bubuk kacang tersebut dibuat dari kacang goreng yang digiling kasar dan biasanya dibumbui gula pasir, garam, jeruk purut,kencur dan bawang putih. Ketika dicampur, rasa manis-gurih dari bubuk kacang berpadu sempurna dengan urap sayuran yang bumbunya dari kelapa parut.
 Nasi urap sangat cocok jika disantap dengan ikan wader (ikan sungai
berukuran kecil) yang digoreng garing. Selain itu, masih ada banyak
ragam lauk yang bisa anda pilih semisal ayam goreng, lele goreng, cingur
sapi, empal daging, hati-ampela ayam, babat, iso, paru, telur ceplok,
dll. Di meja makan juga tersedia banyak macam gorengan seperti mentho,
bakwan, tahu, sosis Solo, dsb.
Nasi urap sangat cocok jika disantap dengan ikan wader (ikan sungai
berukuran kecil) yang digoreng garing. Selain itu, masih ada banyak
ragam lauk yang bisa anda pilih semisal ayam goreng, lele goreng, cingur
sapi, empal daging, hati-ampela ayam, babat, iso, paru, telur ceplok,
dll. Di meja makan juga tersedia banyak macam gorengan seperti mentho,
bakwan, tahu, sosis Solo, dsb.
Jika ingin mencoba menu yang lebih unik, anda bisa menggabungkan nasi urap dengan sambal tumpang yang disiramkan di atasnya. Jadilah menu fusion nasi urap sambal tumpang atau sega gudhang sambal tumpang yang menggugah selera. Sambal tumpang (atau sambal lethok) Boyolali memiliki kuah yang lebih kental daripada sambal tumpang versi Salatiga. Isiannya pun hanya menggunakan tahu, tidak ada daging, koyor, ataupun bahan hewani lainnya. Untuk lauknya anda bisa menambahkan irisan empal, paru, atau yang lainnya sesuai selera anda.
 Betapapun istimewanya nasi urap sambal tumpang, alangkah tidak adil
kalau kita mengabaikan soto yang menjadi menu utama warung ini. Soto di
Warung Nggoper adalah jenis soto ndeso yang menggunakan kuah
kaldu tipis dan isian minimalis. Rasanya segar dan ringan di lidah. Soto
daging sapi ini cocok disantap dengan lauk mentho, sate telur puyuh,
sate hati-ampela, atau aneka gorengan yang tersedia di sepanjang meja.
Porsinya terbilang kecil sehingga tak akan terlalu membebani lambung di
pagi hari.
Betapapun istimewanya nasi urap sambal tumpang, alangkah tidak adil
kalau kita mengabaikan soto yang menjadi menu utama warung ini. Soto di
Warung Nggoper adalah jenis soto ndeso yang menggunakan kuah
kaldu tipis dan isian minimalis. Rasanya segar dan ringan di lidah. Soto
daging sapi ini cocok disantap dengan lauk mentho, sate telur puyuh,
sate hati-ampela, atau aneka gorengan yang tersedia di sepanjang meja.
Porsinya terbilang kecil sehingga tak akan terlalu membebani lambung di
pagi hari.
Warung Soto Nggoper juga menyediakan menu minuman yang bergizi dan menyegarkan: susu sapi segar. Anda bisa memesannya sehingga bisa makin meresapi pengalaman kuliner di Boyolali yang dikenal sebagai sentra penghasil susu sapi di Jawa Tengah.
Jam buka: pagi – sore
Lokasi: Jl. Sendang Lawe, Karanggeneng – Boyolali. Sebelah Timur Pasar Sunggingan (yang ada patung sapinya), tidak jauh dari lokasi Soto Seger Mbok Giyem 1
link : http://dhaniandri.blogspot.co.id/2014/12/kuliner-khas-boyolali.html
Jika membaca judul di atas anda pasti menangkap hal yang aneh, di warung soto kok makannya sambal tumpang? Tapi memang begitulah adanya. Meski menggunakan nama warung soto, tempat ini juga menyediakan menu nasi urap (sega gudhang) dan sambal tumpang (orang Boyolali menyebutnya sambal lethok) yang popularitasnya bahkan mengalahkan menu sotonya.
Urap khas Boyolali (orang Jawa menyebutnya gudhangan) terasa istimewa karena di atasnya ditambahkan taburan bubuk kacang yang memunculkan citarasa khas nan sedap. Bubuk kacang tersebut dibuat dari kacang goreng yang digiling kasar dan biasanya dibumbui gula pasir, garam, jeruk purut,kencur dan bawang putih. Ketika dicampur, rasa manis-gurih dari bubuk kacang berpadu sempurna dengan urap sayuran yang bumbunya dari kelapa parut.
Mentho
khas Boyolali yang terbuat dari parutan kelapa dan kacang tanah /
kacang tolo. Digoreng garing, hingga terasa renyah sampai bagian dalam.
Di tempat lain makanan ini mungkin disebut Lentho
Jika ingin mencoba menu yang lebih unik, anda bisa menggabungkan nasi urap dengan sambal tumpang yang disiramkan di atasnya. Jadilah menu fusion nasi urap sambal tumpang atau sega gudhang sambal tumpang yang menggugah selera. Sambal tumpang (atau sambal lethok) Boyolali memiliki kuah yang lebih kental daripada sambal tumpang versi Salatiga. Isiannya pun hanya menggunakan tahu, tidak ada daging, koyor, ataupun bahan hewani lainnya. Untuk lauknya anda bisa menambahkan irisan empal, paru, atau yang lainnya sesuai selera anda.
Nasi Urap Sambal Tumpang di Warung Soto Nggoper Boyolali. Menggunakan lauk irisan empal daging dan ikan wader goreng
Warung Soto Nggoper juga menyediakan menu minuman yang bergizi dan menyegarkan: susu sapi segar. Anda bisa memesannya sehingga bisa makin meresapi pengalaman kuliner di Boyolali yang dikenal sebagai sentra penghasil susu sapi di Jawa Tengah.
Jam buka: pagi – sore
Lokasi: Jl. Sendang Lawe, Karanggeneng – Boyolali. Sebelah Timur Pasar Sunggingan (yang ada patung sapinya), tidak jauh dari lokasi Soto Seger Mbok Giyem 1
link : http://dhaniandri.blogspot.co.id/2014/12/kuliner-khas-boyolali.html
makanan khas boyolali (MARNING)
hallo teman,kali ini saya akan membahas proses pembuatan salah satu makanan khas daerah saya,BOYOLALI.yang akan saya bahas kali ini adlah proses pembuatan MARNING.
monggo langsung mawon.. :)
Cara membuat marning jagung tidaklah sulit dan rumit, hanya dalam
proses pembuatan marning jagung dibutuhkan waktu yang cukup lama,
sehingga dibutuhkan ketelatenan didalam proses pembuatannya.
Agar mendapatkan rasa yang gurih dan renyah tergantung pada proses pembuatannya, proses pengkapuran, perendaman perebusan, dan yang tidak kalah pentingnya adalah waktu penggorengan. Dari serangkaian proses tersebut harus seimbang dan dilakukan dengan sebaik baiknya agar mengdapatkan hasil yang memuaskan
Langkah langkah yang harus diperhatikan dalam membuat marning jagung.
Pertam: kita pilih bahan baku yang terbaik, yakni memilih biji jagung yang terbaik. Ciri cirinya antara lain biji jagung yang bersih, yang mengkilat, yang benar benar biji jagung yang sudah tua.

Kedua: menyiapkan alat alat pemasakan marning, misalnya kompor yang memiliki bara api yang besar, penggorengan, wadah perebusan jagung, ember untuk perendaman jagung, dan alat untuk mencuci jagung misalnya TOMPO BAMBU.
Proses pemasakan marning jagung
Langkah Pertama: Jagung direbus setengah matang saja, atau sekitaqr 1 jam perebusan, dan air yang digunakan untuk merebus jagung dikasih atau dicampur dengan kapursirih, gunanya untuk membersihkan jagung pada saat di rebus.
WAKTU PEREBUSAN JAGUNG

Langkah Kedua: setelah jagung selesai direbus hingga setengah matang saja, terus jagung di angkat dan dicuci untuk menghilangkan kotoran jagung yang terurai oleh kapur sirih, cuci hingga bersih setelah melewati proses pencucian dan jagung sudah terlihat bersih, pindahkan ke ember atau timba untuk dilakukan perendaman, jadi jagung dimasukkan ke ember atau timba lalu dikasih air sampai diatas volime jagung. Rendam jagung tersebut selama 24 JAM.
PROSES PERENDAMAN

Langkah ketiga: setelah di rendam, jagung dicuci kembali sampai bersih, setelah itu jagung siap di goring. Proses penggorengannya tidaklah sulit, cukup siapkan wajan dan minyak panaskan dengan bara api yang besar setelah itu masukkan jagungnya, terus tinggal di aduk aduk jangn sampai gosong
PROSES PENGGORENGAN

monggo langsung mawon.. :)
CARA MEMBUAT MARNING JAGUNG
Agar mendapatkan rasa yang gurih dan renyah tergantung pada proses pembuatannya, proses pengkapuran, perendaman perebusan, dan yang tidak kalah pentingnya adalah waktu penggorengan. Dari serangkaian proses tersebut harus seimbang dan dilakukan dengan sebaik baiknya agar mengdapatkan hasil yang memuaskan
Langkah langkah yang harus diperhatikan dalam membuat marning jagung.
Pertam: kita pilih bahan baku yang terbaik, yakni memilih biji jagung yang terbaik. Ciri cirinya antara lain biji jagung yang bersih, yang mengkilat, yang benar benar biji jagung yang sudah tua.

Kedua: menyiapkan alat alat pemasakan marning, misalnya kompor yang memiliki bara api yang besar, penggorengan, wadah perebusan jagung, ember untuk perendaman jagung, dan alat untuk mencuci jagung misalnya TOMPO BAMBU.
Proses pemasakan marning jagung
Langkah Pertama: Jagung direbus setengah matang saja, atau sekitaqr 1 jam perebusan, dan air yang digunakan untuk merebus jagung dikasih atau dicampur dengan kapursirih, gunanya untuk membersihkan jagung pada saat di rebus.
WAKTU PEREBUSAN JAGUNG

Langkah Kedua: setelah jagung selesai direbus hingga setengah matang saja, terus jagung di angkat dan dicuci untuk menghilangkan kotoran jagung yang terurai oleh kapur sirih, cuci hingga bersih setelah melewati proses pencucian dan jagung sudah terlihat bersih, pindahkan ke ember atau timba untuk dilakukan perendaman, jadi jagung dimasukkan ke ember atau timba lalu dikasih air sampai diatas volime jagung. Rendam jagung tersebut selama 24 JAM.
PROSES PERENDAMAN

Langkah ketiga: setelah di rendam, jagung dicuci kembali sampai bersih, setelah itu jagung siap di goring. Proses penggorengannya tidaklah sulit, cukup siapkan wajan dan minyak panaskan dengan bara api yang besar setelah itu masukkan jagungnya, terus tinggal di aduk aduk jangn sampai gosong
PROSES PENGGORENGAN

SELAMAT MENCOBA
atom C primer, sekunder, tersier, dan kuarterner
Apa yang dimaksud atom C primer, sekunder, tersier, dan kuarterner? Mungkin sobat baru
mendengar istilah itu sekarang. Untuk memahaminya, sobat dapat melihat struktur
karbon berikut ini.
Keterangan:
|
P = Primer
|
S = Sekunder
|
|
T = Tersier
|
|
K = Kuarterner
|
Dari struktur diatas, berdasarkan jumlah atom karbon yang
terikat pada atom karbon lainnya, apa yang dapat sobat Materi Kimia SMA
simpulkan tentang atom C primer, C sekunder, C tersier, dan C
kuarterner?
- Atom karbon primer (dilambangkan dengan 1°) adalah atom-atom karbon yang mengikat satu atom karbon tetangga.
- Atom karbon sekunder (dilambangkan dengan 2°) adalah atom-atom karbon yang mengikat dua atom karbon tetangga.
- Atom karbon tersier (dilambangkan dengan 3°) adalah atom-atom karbon yang mengikat tiga atom karbon tetangga.
- Atom karbon kuarterner (dilambangkan dengan 4°) adalah atom-atom karbon yang mengikat empat atom karbon tetangga.
kekhasan atom karbon
Apa yang teman teman ketahui tentang atom karbon? Coba sobat
lihat di Sistem Periodik, berada di golongan dan perioda berapa atom karbon
tersebut? Bagaimana dengan konfigurasi elektronnya?


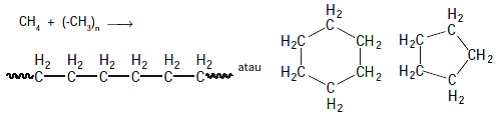
Atom karbon memiliki empat elektron valensi, keempat
elektron valensi tersebut dapat membentuk empat ikatan kovalen melalui
penggunaan bersama pasangan elektron dengan atom-atom lain. Atom karbon dapat
berikatan kovalen tunggal dengan empat atom hidrogen membentuk molekul metana
(CH4).
Rumus Lewisnya:

Mungkin sobat Materi Kimia SMA sudah mengetahui bahwa selain
dapat berikatan dengan atom-atom lain, atom karbon dapat juga berikatan kovalen
dengan atom karbon lain, baik ikatan kovalen tunggal maupun rangkap dua dan
tiga.

H−C≡C−H
Kecenderungan atom karbon dapat berikatan dengan atom karbon
lain memungkinkan terbentuknya senyawa karbon dengan berbagai struktur
(membentuk rantai panjang atau siklik). Hal inilah yang menjadi ciri khas atom
karbon.

Jika satu atom hidrogen pada metana (CH4) diganti
oleh gugus –CH3 maka akan terbentuk etana (CH3–CH3).
Jika atom hidrogen pada etana diganti oleh gugus –CH3 maka akan
terbentuk propana (CH3–CH2–CH3) dan seterusnya
hingga terbentuk senyawa karbon berantai atau siklik.
TATA NAMA SENYAWA DAN PERSAMAAN REAKSI SEDERHANA
- Rumus Kimia
Rumus
kimia adalah lambang molekul unsur atau senyawa yang menyatakan jenis dan
jumlah relatif atom-atom yang terdapat dalam suatu zat.
Contoh;
- Molekul gas oksigen terdiri atas 2 atom O. Rumus kimia gas oksigen adalah O2
- Molekul air terdiri atas 2 atom hidrogen (indeks H = 2) dan 1 atom oksigen. Rumus kimia air adalah H2O dan lambangnya ditulis H2O.
- Molekul asam cuka terdiri atas 2 atom karbon, 4 atom hidrogen, dan 2 atom oksigen. Rumus kimia asam cuka adalah CH3COOH.
- Rumus kimia amonium sulfat adalah (NH4)2SO4. Artinya setiap molekul amonium sulfat terdiri atas 2 atom nitrogen (N), 8 atom hidrogen (H), 1 atom belerang (S), dan 4 atom oksigen (O).
Rumus
kimia sering dinyatakan dalam rumus molekul dan rumus empiris. Rumus molekul
adalah rumus kimia yang menyatakan jenis dan jumlah atom yang membentuk molekul
senyawa. Rumus empiris atau rumus perbandingan menyatakan perbandingan paling
sederhana jumlah atom-atom penyusun senyawa tersebut.
- Tata Nama Senyawa
Sistem
penamaan senyawa kimia dibedakan menjadi dua, yaitu penamaan untuk senyawa
organik dan senyawa anorganik. Penamaan senyawa-senyawa ini didasarkan pada
rumus kimia dengan aturan-aturan tertentu. Aturan penamaan senyawa anorganik
adalah,
- Tata Nama Senyawa Biner
- Senyawa Biner yang Terdiri atas Unsur Logam dan Nonlogam
Aturan
penamaan;
- Unsur yang berada di depan (logam) diberi nama sesuai dengan nama unsur tersebut
- Unsur yang berada di belakang (nonlogam) diberi nama sesuai dengan nama unsur tersebut dengan menambahkan akhiran – ida.
Contoh;
KCl nama, kalium klorida
- Muatan kation ditulis menggunakan angka Romawi(jika diperlukan). Unsur logam sebagai kation (ion positif) dan unsur nonlogam (ion negatif). Penulisan angka Romawi berlaku apabila unsur logam di dalamnya memiliki kation lebih dari satu macam.
Contoh;
Logam Fe
memiliki kation Fe2+ dan Fe3+ sehingga penulisan nama
senyawa FeCl3 : besi (III) klorida.
Rumus umum
penggabungan kation dan anion pada senyawa biner.
Xa+
+ Yb-→ XbYa
Keterangan;
Xa+ = kation
Yb-
= anion
Perhatikan
beberapa contoh berikut;
Mg2+
+ Cl–→ MgCl2
Ag+ +
Br–→ AgBr
Na+
+ O2-→ Na2O
- Senyawa Biner yang Terdiri Atas Unsur Nonlogam dan Nonlogam
Aturan
penamaannya ditandai dengan awalan angka Yunani yang menyatakan jumlah atom
nonlogam diikuti dengan nama unsur dan diakhiri dengan akhiran- ida.
Awalan
angka Yunani:
Mono
: 1
Di :
2
Tri :
3
Tetra :
4
Penta :
5
Heksa :
6
Hepta :
7
Okta :
8
Nona :
9
Deka :
10
Awalan mono
hanya dipakai pada unsur nonlogam yang kedua.
Penulisan
dilakukan berdasarkan urutan; B- Si- As- C- P- N- H- S- I- Br- Cl- O- F
Contoh;
CO =
karbon monoksida
CO2
= karbon dioksida
N2O5
= dinitrogen pentaoksida
- Tata Nama Senyawa Poliatom
Senyawa
poliatom adalah senyawa yang terdiri atas lebih dari dua macam unsur penyusun
yang berbeda. Kebanyakan ion poliatom bermuatan negatif, kecuali ion amonium
(NH4+)
yang bertindak sebagai kation. Penamaan senyawa poliatom sama dengan aturan
penamaan senyawa biner logam dan nonlogam. Naqmun terdapat perbedaan pada
penamaan anionnya sebagai berikut.
- Anion yang terdiri dari atom penyusun yang sama, untuk jumlah oksigen yang lebih sedikit diberi akhiran-it, dan untuk jumlah oksigen yang lebih banyak diberi akhiran-at.
Contoh;
SO32-
: sulfit
SO42-
: sulfat
- Khusus untuk CN– dan OH– mendapat akhiran-ida.
- Anion yang mengandung unsur golongan VIIA (F, Cl, Br, dan I), urutan penamaan anion dengan jumlah oksigen terkecil sampai terbesar, yaitu: hipo + nama unsur + akhiran-it,
Nama unsur
+ akhiran –it, nama unsur + akhiran –at, sampai per + nama unsur + akhiran –at.
Contoh:
ClO–
: hipoklorit
ClO2–
: klorit
ClO3–
: klorat
ClO4–
: perklorat
Rumus umum
penggabungan kation dan anion pada senyawa poliatom:
Xa+
+ YZb-→ Xb(YZ)a
Contoh:
NH4+
+ Cl–→ NH4Cl : amonium klorida
K+
+ CN–→ KCN : kalium sianida
Zn2+
+ OH–→ Zn(OH)2 : seng hidroksida
Fe3+
+ SO42-→ Fe2(SO4)3 :
besi (III) sulfat
Mg2+
+ SO42-→ MgSO4 : magnesium sulfat
Tidak
ditulis Mg2(SO4)2, karena rumus empirisnya
MgSO4.
- Tata Nama Senyawa Asam
Asam
adalah zat yang di dalam air larut dan terurai menghasilkan ion hidrogen (H+)
dan ion negatif. Semua asam diberi nama dengan awalan asam yang diikuti nama
ion negatifnya.
Contoh:
Asam-asam
anorganik atau asam mineral.
HF = asam
fluorida
H2SO4
= asam sulfat
HClO2
= asam hipoklorit
HClO3
= asam klorit
HClO4
= asam perklorat
HNO3
= asam nitrat
H2C2O4
= asam oksalat
H3PO3
= asam fosfit
H3PO4
= asam fosfat
H2CrO4
= asam kromat
H2Cr2O7
= asam dikromat
H2CO3
= asam karbonat
Contoh
asam-asam organik, yaitu asam yang diperoleh dari hewan dan tumbuhan diberi
nama dengan nama trivial.
HCOOH asam
format
C6H8O7
asam sitrat
C4H6O5
asam malat
C4H4O6
asam tartarat
C4H6O2
asam butirat
C4H12O2
asam kaproat
C6H8O6
asam askorbat
- Tata Nama Senyawa Basa
Basa
ditandai dengan adanya ion hidroksida (OH–). Penamaan basa selalu
diakhiri dengan anion hidroksida.
Contoh:
NaOH natrium hidroksida
Ba(OH)2
barium hidroksida
NH4OH
amonium hidroksida
- Oksida dan Tata Nama Oksida
Oksida
adalah senyawa berupa unsur dan oksigen yang terbentuk pada peristiwa oksidasi.
Secara umum oksida dibedakan menjadi oksida logam dan oksida nonlogam.
Berdasarkan sifat-sifatnya, oksida dibagi menjadi oksida basa, oksida asam,
oksida amfoter, oksida indifferen, dan peroksida.
- Oksida basa adalah oksida logam yang dengan air akan menghasilkan basa atau hidroksida.
Contoh: Na2O
+ H2O → 2NaOH
Natrium
oksida natrium hidroksida
- Oksida asam adalah oksida nonlogam yang bereaksi dengan air akan menghasilkan asam.
Contoh: CO2
+ H2O → H2CO3
Karbon
dioksida asam karbonat
- Oksida amfoter adalah oksida logam atau nonlogam yang dapat bersifat sebagai oksida asam atau oksida basa.
Contoh: Al2O3
(aluminium oksida) dan PbO (timbal oksida)
- Oksida Indifferen adalah oksida logam atau nonlogam yang tidak bersifat sebagai oksida asam ataupun oksida basa.
Contoh: H2O
(air), NO (nitrogen monoksida), dan MnO2 (mangan dioksida)
- Peroksida adalah oksida logam atau oksida nonlogam yang kelebihan atom O.
Contoh: H2O2
(hidrogen peroksida) dan Na2O2 (natrium peroksida).
Pemberian nama senyawa oksida
berdasarkan IUPAC (International Union Of Pure Applied Chemistry) sebagai
berikut.
- Untuk senyawa oksida yang tersusun atas unsur yang mempunyai bilangan oksidasi hanya satu macam, pemberian nama dilakukan dengan menyebutkan nama unsurnya yang kemudian dibutuhkan kata oksida.
Contoh:
- Senyawa Al2O3 tersusun atas unsur Al yang hanya mempunyai bilangan oksidasi +3 dinamai senyawa aluminium oksida.
- Senyawa Na2O yang tersusun atas unsur Na yang hanya mempunyai bilangan oksidasi +1 dinamai senyawa natrium oksida.
- Untuk oksida yang tersusun atas unsur logam yang mempunyai bilangan oksidasi lebih dari satu macam, pemberian nama dilakukan dengan menyebutkan nama unsur logamnya yang diikuti dengan tingkat bilangan oksidanya yang ditulis dengan angka Romawi dalam kurung dan diikuti kata oksida.
Contoh:
- Senyawa oksida tembaga dapat terbentuk dari unsur tembaga yang mempunyai bilangan oksidasi +1 (Cu2O) dan +2(CuO), sehingga senyawa Cu2O dinamakan senyawa tembaga (I) oksida dan senyawa CuO dinamakan senyawa tembaga (II) oksida.
- Senyawa oksida besi dapat terbentuk dari unsur besi yang mempunyai bilanagan oksidasi +2 (FeO) dan +3 (Fe2O3), sehingga senyawa FeO dinamakan besi (II) oksida dan senyawa Fe2O3 dinamakan besi (III) oksida.
- Untuk senyawa oksida yang tersusun atas unsur nonlogam yang mempunyai bilangan oksidasi lebih dari satu macam, pepberian nama dilakukan dengan menyebutkan jumlah atom unsur dan oksida yang terikat pada unsur dengan awalan .
Contoh:
- Senyawa oksida klor dapat terbentuk dari unsur klor yang mempunyai bilangan oksidasi +1(Cl2O), +5(Cl2O5), dan +7(Cl2O7), sehingga nama senyawa tersebut berturut-turut adalah diklor monoksida, diklor pentaoksida dan diklor heptaoksida.
- Senyawa oksida nitrogen dapat terbentuk dari unsur nitrogen yang mempunyai bilangan oksidasi +1 (N2O), +2 (NO), +4 (NO2), dan +5 (N2O5), sehingga senyawa N2O5 dinamakan dinitrogen pentaoksida.
- Tata Nama Senyawa Hidrat
Beberapa
senyawa yang berwujud kristal mampu mengikat air dari udara atau bersifat
higroskopis, sehingga kristal senyawa tersebut mengandung “air kristal” .
Senyawa yang mengandung air kristal disebut hidrat. Kristal hidrat tidak berair
karena molekul air terkurung rapat dalam kristal senyawa. Senyawa hidrat
dibeeri nama dengan menambahkan angka Yunani yang menyatakan banyaknya air
kristal hidrat diakhir nama senyawa tersebut.
Contoh:
CuSO4
. 5H2O = Tembaga (II) sulfat pentahidrat
Na2CO3
. 10H2O = Natrium karbonat dekahidrat
- Beberapa Senyawa Kimia di Sekitar Kita
Beberapa
senyawa kimia yang serin ditemui dalam kehidupan sehari- hari sebagai berikut.
- Dacron atau poliethiena glikol tereftalat dengan rumus molekul (C10H8O4)n . Dacron digunakan sebagai busa pada peralatan rumah tangga, seperti bantal dan kasur.
- Freon atau dicloro difluoro karbon, dengan rumus molekul CCl2F2 digunakan sebagai bahan pendingin lemari es dan AC, serta pengisi obat semprot (spay).
- Kloroform atau triklorometana, dengan rumus molekul CHCl3. Kloroform pada suhu kamar berupa zat cair, berbau, mudah menguap, dan bersifat membius.
- DDT atau dikloro difenil trikloro etana, dengan rumus molekul C14H9Cl5 , digunakan sebagai pestisida.
- PVC atau polivinil klorida, dengan rumus molekul (H2CCClH)n . Digunakan untuk membuat pipa pralon, pembungkus kabel, dan tas plastik.
- Teflon atau tetrafluoroetena, dengan molekul (F2C = CF2)n. Sifatnya sangat keras dan tahan panas, sehingga banyak digunakan sebagai pengganti logam pada peralatan mesin-mesin dan peralatan rumah tangga.
- Aseton, mempunyai rumus kimia CH3COOCH3 dipakai sebagai pelarut pada industri selulosa asetat, serat, fotografi film, cat, dan pernis serta digunakan sebagai pembersih cat kuku.
- Persamaan Reaksi
Persamaan
reaksi menggambarkan reaksi kimia yang terdiri atas rumus kimia pereaksi
(reaktan) dan hasil reaksi (produk) yang dipisahkan dengan tanda (→) disertai
koefisiennya masing-masing.
Prinsip
yang mendasari penulisan persamaan reaksi adalah hukum kekekalan massa oleh
Lavoisier. Hukum ini menyatakan bahwa massa sebelum reaksi sama dengan massa
ssudah reaksi. Dengan demikian, persamaan reaksi disetarakan dengan
syarat-syarat sebagai berikut.
- Jenis unsur-unsur sebelum dan sesudah reaksi selalu sama
- Pereaksi dan hasil reaksi dinyatakan dengan rumus kimia yang benar. Pereaksi ditulis di sebelah kiri tanda panah, sedangkan hasil reaksi ditulis di sebelah kanan tanda panah.
Contoh : A
+ B → C + D
- Persamaan reaksi pembakaran senyawa organik dengan menambahkan O2, yaitu :
- Reaksi pembakaran sempurna menghasilkan CO2 dan H2O
- Reaksi pembakaran tidak sempurna menghasilkan CO dan H2O
- Perasamaan reaksi harus memenuhi hukum Kekekalan Massa. Apabila jumlah unsur di sebelah kiri tanda panah berbeda dengan jumlah unsur di sebelah kanan, ditambahkan angka sebagai koefisien reaksi di depan senyawa yang berhubungan. Perbandingan koefisien reaksi menyatakan perbandingan mol.
Contoh:
H2
+ O2→ H2O (belum setara)
Setelah
ditambahkan angka menjadi
2H2O
+ O2→ 2H2O
- Pada reaksi yang kompleks, penyetaraan reaksi dilakukan dengan cara aljabar, yaitu dengan menggunakan variabel-variabel sebagai koefisien senyawa.
Contoh:
aHNO3
+ bH2S → cNO + dS + eH2O
atom N : a
= c (sebelum dan sesudah reaksi)
atom O :
3a = c + e, karena a = c, maka
3a = a + e
2a = e
Atom H : a
+ 2b = 2e, karena e = 2a, maka:
a + 2b =
2(2a)
2b = 4a –
a
2b = 3a
b = a
atom S : b
= d = a
Misal a =
2, persamaan reaksi tersebut menjadi:
2HNO3
+ 3H2S → 2NO + 3S + 4H2O
- Wujud zat-zat yang terlibat reaksi harus dinyatakan dalam tanda kurung setelah rumus kimia. Wujud zat dalam persamaan reaksi disingkat dengan:
(s) :
solid (zat padat)
(l) : liquid
(zat cair)
(aq) :
aqueous (larut dalam air)
(g) : gas
Contoh:
2HNO3(aq)
+ 3H2S(aq) → 2NO(g) + 3S(s) + 4H2O(l)
BAB V HUKUM DASAR KIMIA
- Hukum Kekekalan Massa (Hukum Lavoisier)
Hukum
kekekalan massa menyatakan bahwa, “Massa zat-zat sebelum dan sesudah reaksi
adalah tetap”.
Contoh:
hidrogen + oksigen → hidrogen oksida
(4g) (32g)
(36g)
- Hukum Perbandingan Tetap (Hukum Proust)
Proust
mengemukakan teorinya yang dikenal dengan hukum perbandingan tetap yang
berbunyi; “Perbandingan massa unsur-unsur penyusun suatu senyawa selalu tetap”
Contoh:
Jika 4
gram hidrogen dengan 40 gram oksigen, berapa gram air yang terbentuk?
Penyelesaian:
Perbandingan
massa hidrogen dengan oksigen = 1 : 8
Perbandingan
massa hidrogen dengan oksigen yang dicampurkan = 4 : 40
Oleh
karena perbandingan hidrogen dan oksigen = 1 : 8 maka 4 gr hidrogen memerlukan
4 x 8
Gram
oksigen yaitu 32 gram.
Pada kasus
ini oksigen yang dicampurkan tidak bereaksi semuanya, oksigen masih bersisa
sebanyak (40 – 32) gram = 8 gram
Langganan:
Postingan (Atom)
